Газы, в отличие от жидкостей и твёрдых тел, не обладают формой. Если газ поместить в какой-нибудь сосуд, то он займёт весь его объём.

Это связано с тем, что молекулы газа почти не взаимодействуют друг с другом. Из-за этого механизм давления газов существенно отличается от механизмов давления жидких и твёрдых тел.
Поставим гирю на стол и рассмотрим её взаимодействие со столом на молекулярном уровне.

Под действием силы тяжести, молекулы гири сближаются с молекулами стола. Расстояние между ними уменьшается до тех пор, пока гирю не удержат силы отталкивания молекул друг от друга. Силы, с которыми молекулы гири действуют на молекулы стола, очень маленькие. Но количество молекул огромное. Маленькие силы складываются, и получается равнодействующая сила. В данном случае, равнодействующая сила – это вес гири. Получается вес – это сила давления гири на стол, иначе говоря, твёрдого тела на твёрдое тело.
Если силу давления разделить на площадь, по которой она распределена, то получится давление.
В газах происходит по-другому.
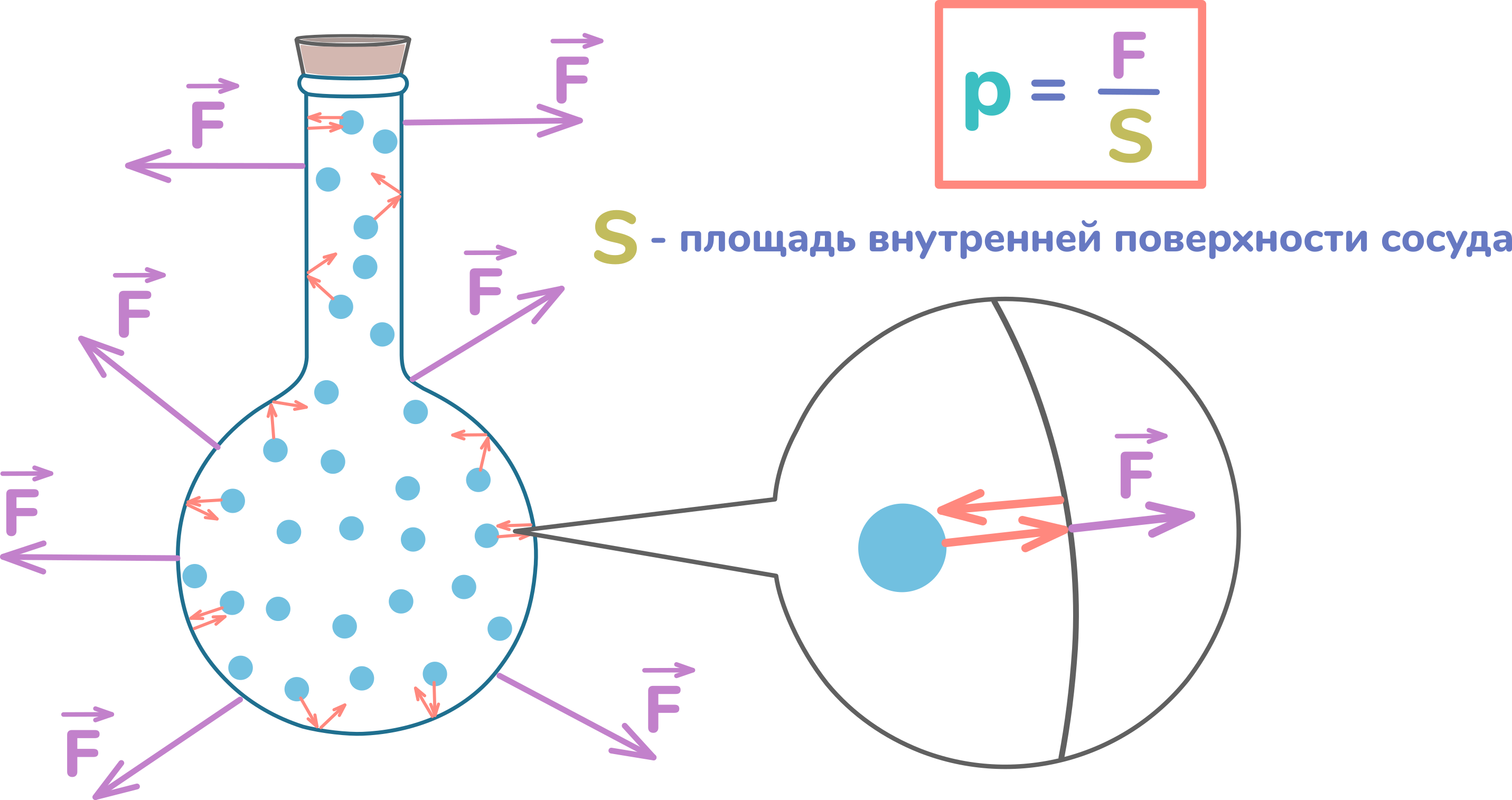
Молекулы газа беспорядочно разлетаются по пространству. Если газ запустить в сосуд, и закрыт его, газ останется в сосуде. Это значит, когда его молекулы разлетаются, они натыкаются на стенки сосуда, и, ударяясь о них, возвращаются обратно. Получается, при ударе, молекула действует с какой-то силой на стенку сосуда. Эта сила крошечная, а её действие кратковременное. Но молекул огромное количество, поэтому суммарная сила их ударов может быть очень большой. Это и есть сила давления газов. Разделив эту силу на площадь её воздействия, получаем давление газа. S, в данном случае, это площадь внутренней поверхности сосуда.
Получается, что давление газа на стенки сосуда или на помещённое в газ тело, вызвано ударами молекул газа.
Окружающий нас воздух – это газ. Его молекулы также постоянно ударяются об окружающие нас предметы. Например, если в помещении подвесить лист бумаги, молекулы воздуха будут ударяться также и об него.
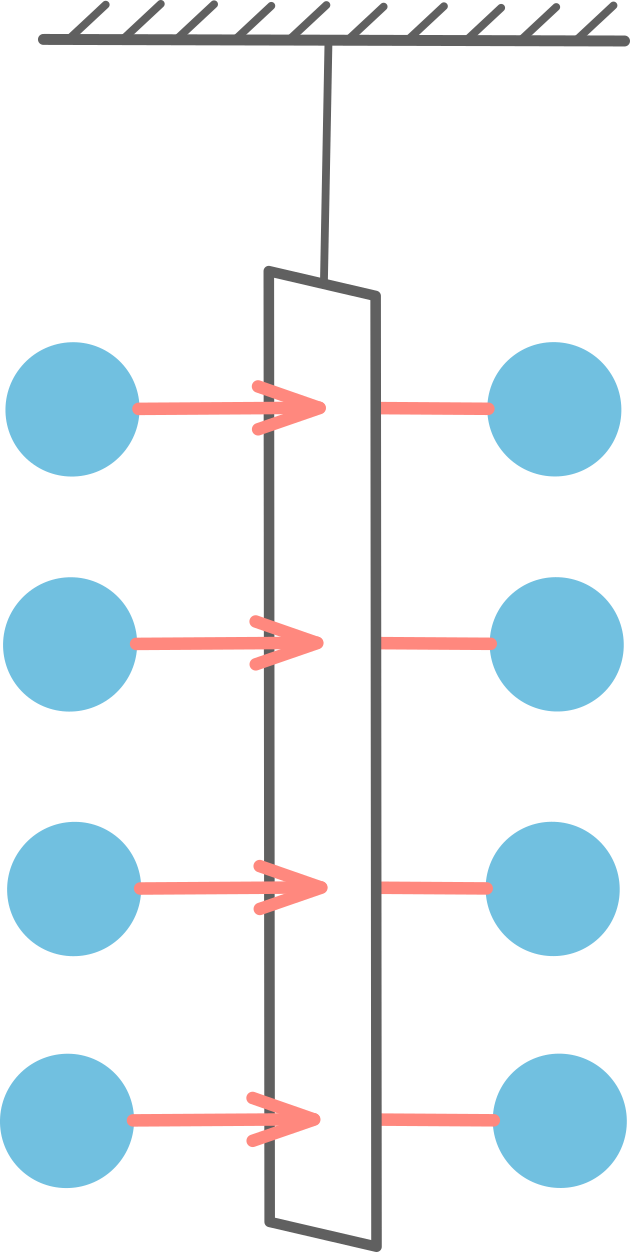
Но если нет сквозняка, лист не будет отклоняться от ударов. Это объясняется тем, что с другой его стороны молекулы также ударяются о него. Равнодействующие силы ударов с обеих сторон равны, а, значит, компенсируют друг друга, поэтому лист остаётся неподвижным.
Чтобы убедиться, что давление возникает из-за ударов молекул газа, рассмотрим следующий опыт. Поместим связанный резиновый шарик под стеклянный колпак.
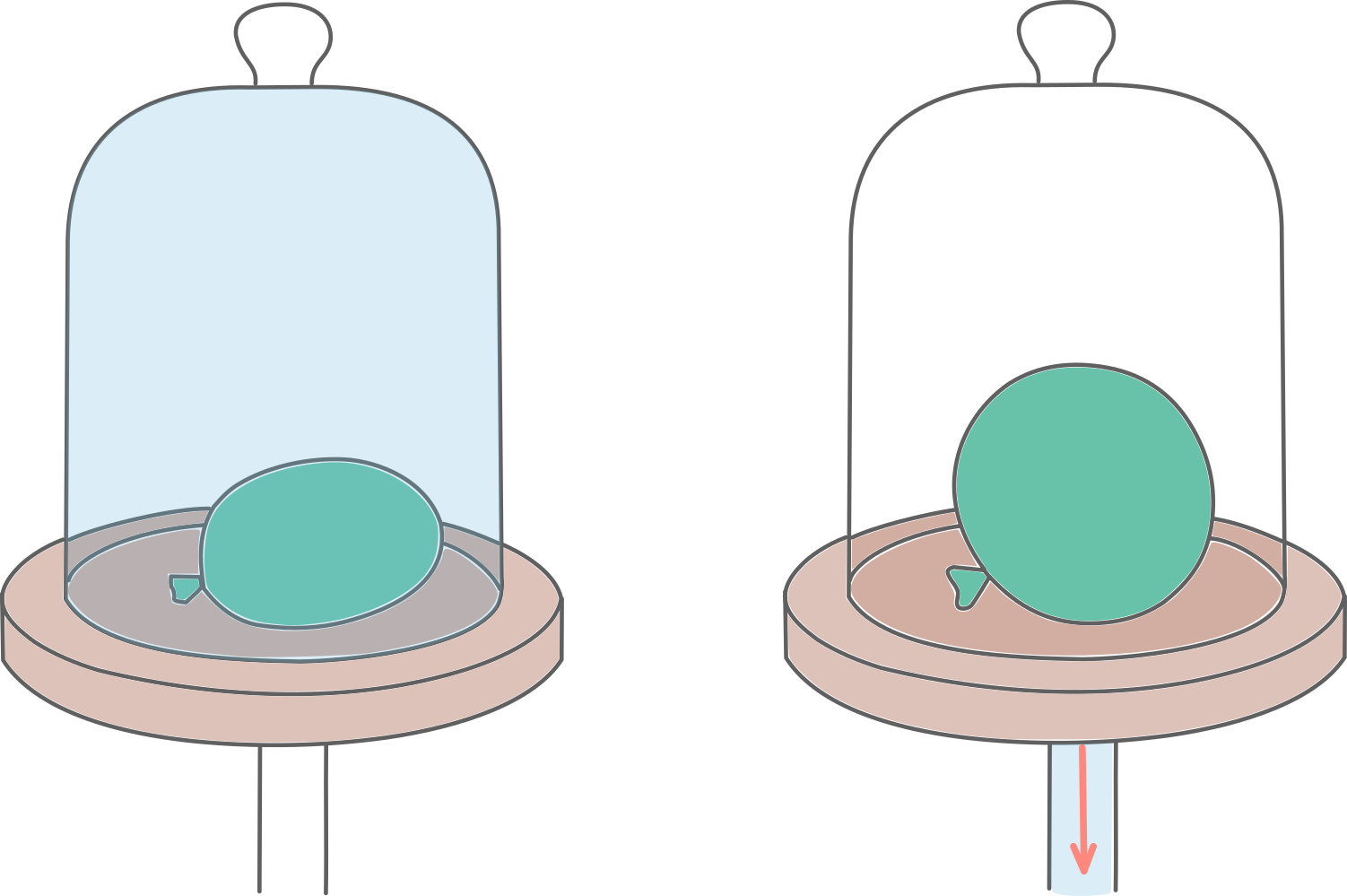
Шарик содержит немного воздуха и имеет некруглую форму. Беспорядочно движущиеся молекулы воздуха ударяются о стенки шарика изнутри и снаружи.
Откачаем насосом из-под колпака воздух. Иначе говоря, уменьшим количество молекул газа, которые бьют шарик снаружи. Так как молекул стало меньше, то и ударов стало меньше. А количество ударов внутри осталось прежнее. От этого оболочка шарика раздувается до тех пор, пока сила упругости его резиновой оболочки не станет равной силе давления газа. При этом раздутая оболочка принимает форму шара. Это показывает, что число ударов молекул на каждый квадратный сантиметр её поверхности по всем направлениям одинаково.
Иначе говоря, газ давит на стенки оболочки по всем направлениям одинаково.
Рассмотрим другой опыт. В стеклянную трубку вставлен поршень. Другой её конец закрыт тонкой резиновой плёнкой. Давление снаружи и внутри одинаковое.
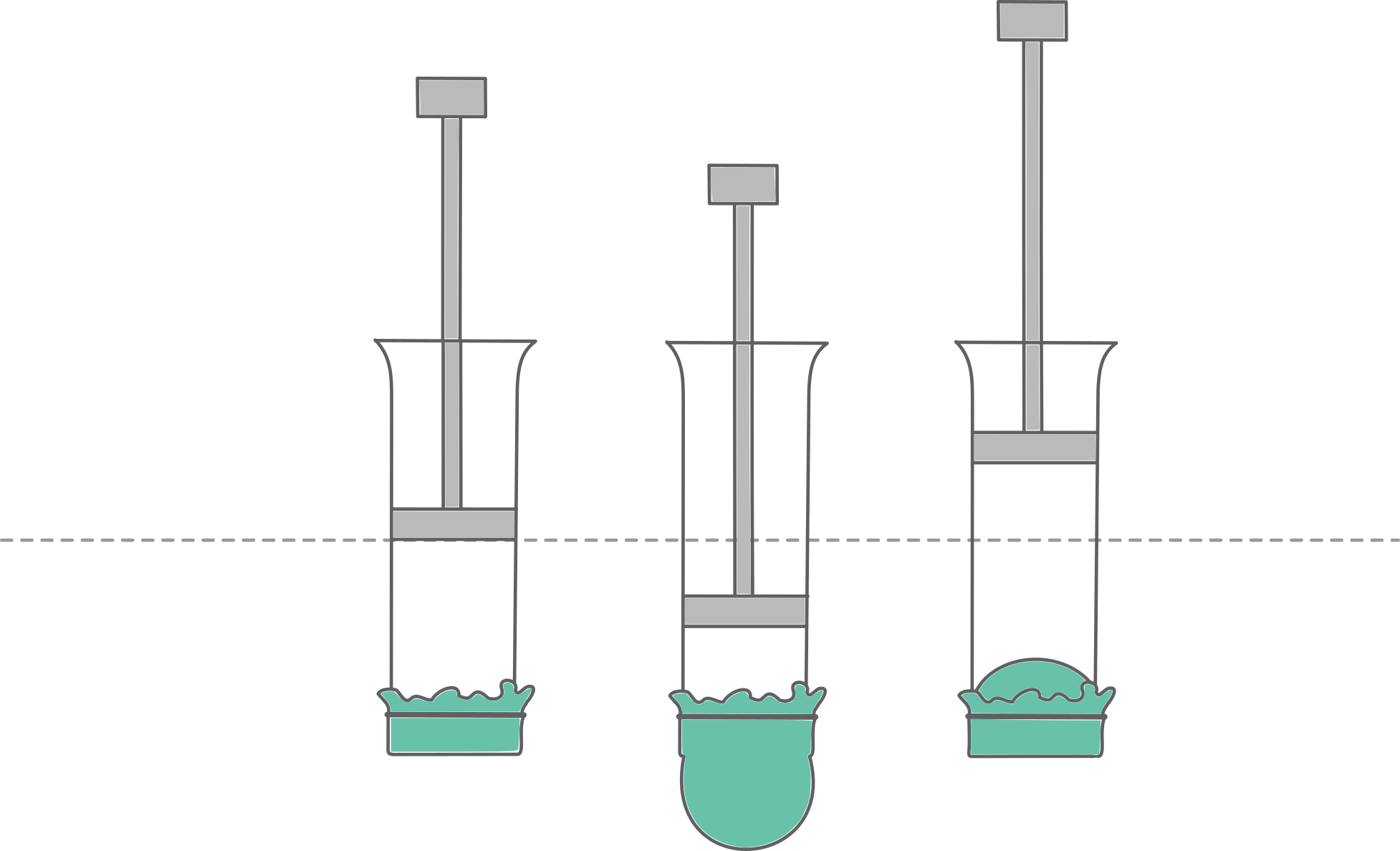
При вдвигании поршня объём воздуха в трубке уменьшается, то есть газ сжимается. Резиновая плёнка при этом выгибается наружу. Это значит, что давление воздуха в трубке увеличилось. Масса воздуха при этом не менялась. Изменился лишь его объём. В результате в каждом кубическом сантиметре газа молекул стало больше, плотность газа увеличилась, молекулы стали чаще ударяться о стенки сосуда и плёнку. А чем больше ударов молекул за единицу времени, тем больше давление.
Если вытянуть поршень, масса воздуха также останется прежней, а объём воздуха увеличится. Плёнка при этом прогибается внутрь трубки. Число молекул в каждом кубическом сантиметре стало меньше. От этого уменьшилось и число ударов молекул о стенки сосуда и плёнку. Атмосферное давление при этом осталось прежним. То есть снаружи стало больше ударов молекул воздуха о трубку и о резиновую плёнку.
Итак, если масса газа остаётся неизменной, то при уменьшении объёма газа его давление увеличивается, а при увеличении объёма давление уменьшается.
Давление газа также зависит от температуры.
Перед вами сосуд с газом. На его конце закреплена тонкая резиновая плёнка. Теперь рассмотрим его в нагретом состоянии.
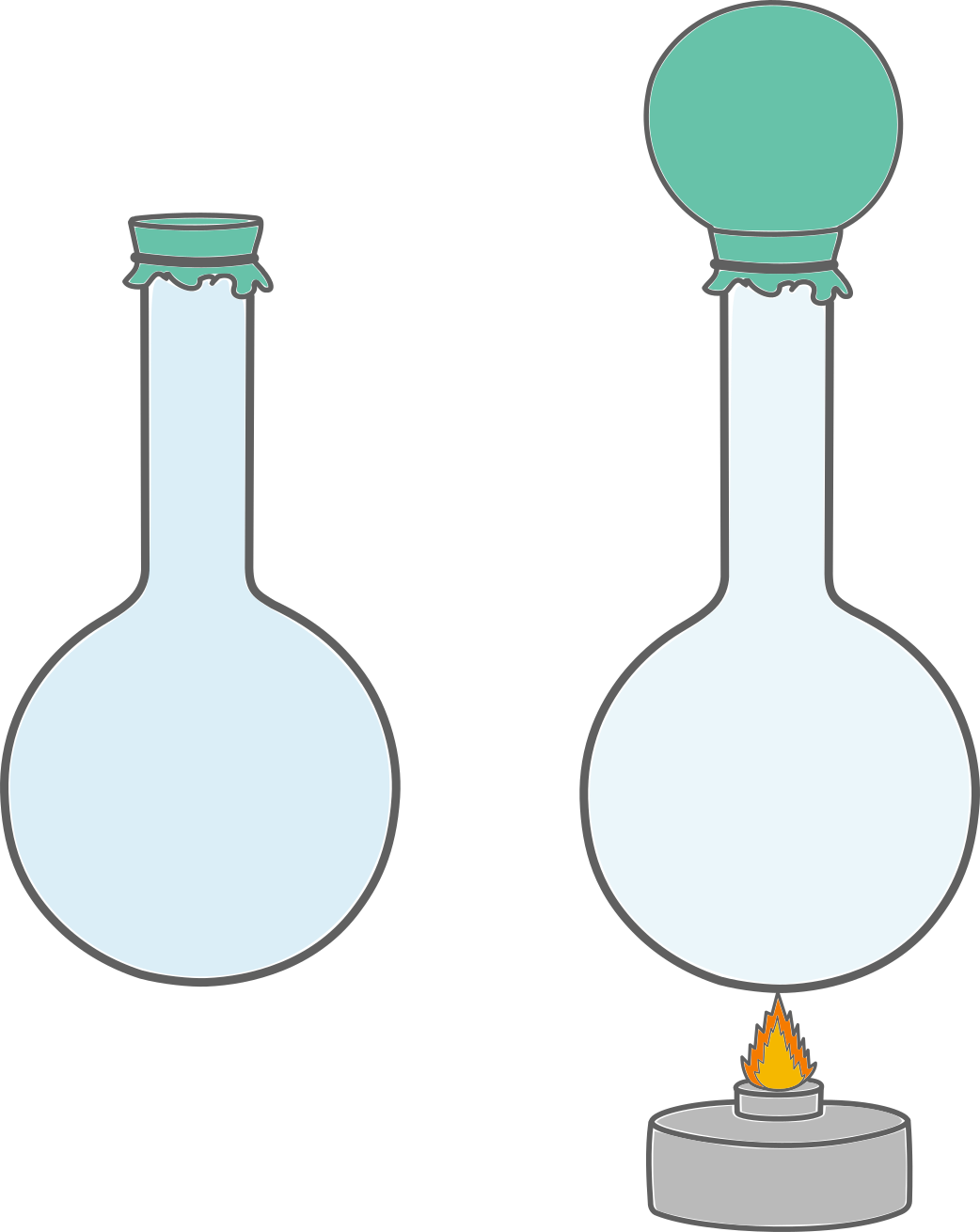
Как при нормальной температуре, так и при высокой, давление газа обусловлено ударами молекул. Количество молекул не изменилось. Объём также остался прежним. Значит, расстояние между молекулами остаётся тем же самым.
Изменилась только скорость движения молекул. С ростом температуры она увеличилась. Следовательно, молекулы ударяются о стенки сосуда чаще и с большей силой. Таким образом, давление газа увеличивается.
Иными словами, с ростом температуры, растёт и давление.